消化科系
簡介肝臟實時融合影像超音波
胃腸肝膽科 資深主治醫師 王勝永
背景與融合影像超音波的原理
超音波在臨床上對於肝臟疾病的診斷與治療扮演著極為重要的角色。由於肝臟超音波能夠方便地提供即時動態影像,因此廣泛運用在臨床上診斷治療肝臟病灶,雖然此檢查評估項目已經相當成熟,在臨床應用上仍有一些難題。臨床上時常可見電腦斷層、核磁共振、與肝臟超音波不同檢查之間各說各話的不一致場景。在電腦斷層或核磁共振影像所解析的影像,一般以橫斷面、冠狀面、或矢狀面為主,如何將該影像所指出的病灶準確的對應到動態超音波影像,傳統上需要超音波操作者將不同切面的影像在大腦裡自行重組並對應到超音波位置,雖然不需要額外的儀器,但需要相當的訓練與經驗,而且容易會有操作者人為誤判。在肝臟超音波掃描時,常會受到肺部空氣與腸氣的干擾影響音波偵測之視窗,小型或不明顯病灶可能會躲在超音波難以偵測的位置,有時操作者會誤判將可視的肝臟區域內的假影或疑似病灶當作是目標病灶治療。
實時融合影像(real-time fusion imaging)超音波可將兩個不同的影像即時地融合在一起,一邊是事前擷取之影像(如電腦斷層、核磁共振、甚至是超音波對比劑影像),另一邊是即時的肝臟超音波影像。主要的原理是利用電磁場產生與接受器,可得知超音波探頭的空間位置與方向,利用電腦運算輔助將不同的影像的空間作標的對應,由於電腦運算能力與軟體技術的進步,可以即時地將事前擷取之影像做解析重組顯示,以致事前擷取的影像會隨著超音波探頭在患者體外移動時與目前擷取的影像動態對應同步。
如何執行肝臟實時融合影像超音波
前置作業包括將患者、影像、機器設置定位。首先需要請患者就定一個可較輕鬆維持一段時間的姿勢,因為在執行實時融合影像超音波時,患者的移動將會影響比對的精確度。接下來是將探頭感應器接好,如果是可移動式的電磁場產生器,需要擺至適當的位置,各家不同廠牌機器使用的技術不盡相同,也因此電磁場產生器的最佳位置也有所差異,最終還是以螢幕顯示的探頭感應強度到可接受的程度才行。此時擷取已存檔在伺服器或儲存媒介的電腦斷層、核磁共振影像。前置作業完成後便開始進行影像融合,首先軟體會啟動電磁場產生器,接著就是擷取動態超音波影像,根據定位點、面、立體資訊的不同,將電腦斷層或核磁共振影像與超音波影像做空間資訊的對應校正,接著兩方的影像即可以融合而實時呈現。
定位點的產生方式一般有下列幾種:一.患者將體外定位點或追縱器帶著接受電腦斷層掃描,接著接受超音波檢查,利用體外追縱器對應不同影像。二.操作者將不同影像間的相同對應點輸入為體內定位點。三.操作者移動超音波探頭得到對應事先擷取的影像(一般是以橫斷面)的類似二維的超音波影像作為定位面。四.較新的技術可以利用超音波探頭擷取三維超音波,電腦運算比對兩個不同的影像的三維空間座標。
肝臟實時融合影像超音波在消融肝腫瘤的應用
肝臟介入性治療尤其是射頻消融術已經在治療早期小型肝細胞癌證實具有相當好的療效,目前在國內外已經為廣泛接受的重要肝癌治療選項。置入治療探針在射頻消融術對於治療效果有直接相關,相較於電腦斷層導引,經超音波導引置入有著經濟性、省時、效率、低放射性等優點。肝臟實時融合影像超音波對於肝臟病灶的介入性治療帶來許多好處。首先,在過去的研究顯示,射頻消融術在實時融合影像超音波協助下,可改善在B mode超音波影像上不明顯的肝細胞癌之偵測,並增進經皮射頻消融術的可能性。另有研究指出,對於2公分以下的小型肝細胞癌,實時融合影像超音波較傳統的B mode超音波有更高的偵測率,在2公分以上的肝細胞癌則無差異。
在射頻消融治療過程中,微型氣泡的產生使得傳統超音波難以即時評估探針的位置與消融的範圍是否適當,實時融合影像可對應事前擷取之影像而瞭解探針與消融的區域是否適當。有時在超音波上難以評估射頻消融治療後的復發或殘餘肝癌病灶,融合影像可將電腦斷層或核磁共振檢查發現的癌病灶實時對應到動態的超音波影像,提升介入性消融治療的可能性與準確度,減少治療之錯誤或可能相關併發症。
肝臟實時融合影像超音波之自動對準系統
相較於早期實時融合影像操作常因電腦運算能力不足帶來操作流程的緩慢與不流暢,目前市場上的多數實時融合影像機種均致力於改善簡化融合工作流程,但是利用定位點或面的方式要達到可接受的肝臟超音波實時融合影像,仍需要相當的學習與經驗,對於困難的案,甚至需要花很長的時間仍無法達到可接受的融合結果。
自動對準(automatic registration)系統為一新的發展能自動化肝臟實時融合影像超音波的對準流程,此技術主要是利用自動三維超音波探頭或者是手動移動二維超音波探頭擷取三維超音波影像,電腦自動分別計算三維超音波影像與斷層掃描的肝內血管走向(需要有顯影劑的掃描影像)或者是肝臟表面輪廓,運算後電腦自動將此兩者三維空間座標匹配對準。在理想狀態下甚至可以在一分鐘內自動地完成影像融合。此一新進展不但大幅減少操作者的進入障礙、改善學習曲線,而且可以減少可能的人為影響、簡化流程、縮短操作時間。
|
|
|
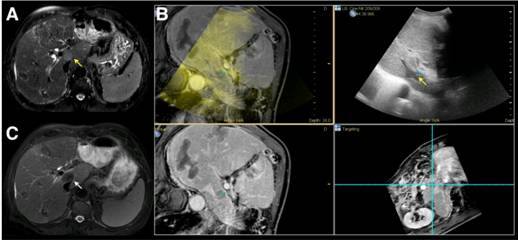
圖一、融合影像肝臟超音波應用於射頻消融肝細胞癌。A.T2核磁共振影像可見一 2公分肝細胞癌於S1(箭頭)。B.超音波所見S1低回音病灶經由融合影像肝臟超音波確認為靜脈相核磁共振影像具早期消褪特徵之病灶(箭頭)。C.患者接受經皮超音波導引射頻消融治療見肝癌病灶達完全消融(箭頭)。 |
總結
肝臟超音波已經是在臨床上不可或缺的重要工具,但對於肝臟病灶的診斷或介入性治療仍有不足之處,肝臟實時融合影像超音波為目前超音波的新進展與趨勢,將動態超音波影像與其他事前擷取之影像同步後,能針對傳統超音波難以評估發現的肝臟病灶做進一步之診斷與介入性治療。近年來此領域的進展使得工作流程大幅簡化且縮短所需要的時間。肝臟實時融合影像超音波可促進消融治療傳統超音波不易甚至是無法處理的肝臟病灶,提升介入性消融治療的可能性與準確度,增進治療效果。
參考文獻
1. Lee MW. Fusion imaging of real-time ultrasonography with CT or MRI for hepatic intervention. Ultrasonography. 2014; 33: 227-239.
2. Song KD, Lee MW, Rhim H, Cha DI, Chong Y, Lim HK. Fusion imaging-guided radiofrequency ablation for hepatocellular carcinomas not visible on conventional ultrasound. AJR Am J Roentgenol. 2013; 201: 1141-1147.
3. Lee MW, Rhim H, Cha DI, Kim YJ, Lim HK. Planning US for percutaneous radiofrequency ablation of small hepatocellular carcinomas (1-3 cm): value of fusion imaging with conventional US and CT/MR images. J Vasc Interv Radiol. 2013; 24: 958-965.
4. Wein W, Brunke S, Khamene A, Callstrom MR, Navab N. Automatic CT-ultrasound registration for diagnostic imaging and image-guided intervention. Medical Image Analysis. 2008; 12: 577-585.
5. Clevert DA, Paprottka PM, Helck A, Reiser M, Trumm CG. Image fusion in the management of thermal tumor ablation of the liver. Clin Hemorheol Microcirc 2012; 52: 205-216.